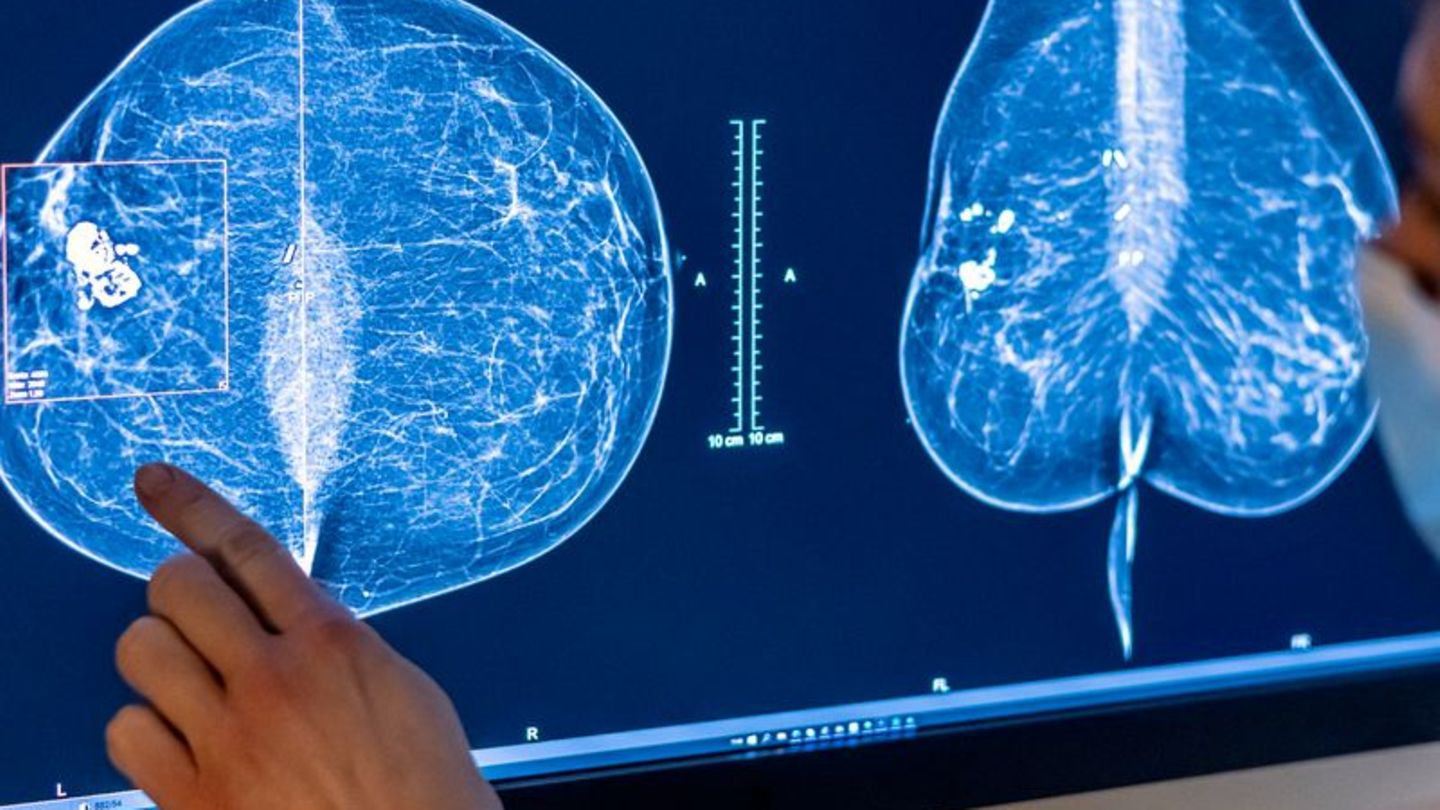
Charlas químicas: Árboles mágicos de plata de una placa de Petri
Usando electricidad y una solución de nitrato de plata, dos árboles muy similares crecen en una placa de Petri. Pero si se mira más de cerca, son fundamentalmente diferentes.
© Grupo de trabajo Marko Oetken, PH Freiburg (detalles)
Los delicados árboles plateados lucen impresionantes en una solución de electrolitos de colores brillantes.
Cuando se electroliza una solución de nitrato de plata, se deposita plata elemental en el cátodo. Si este experimento se realiza en una placa de Petri con un cátodo puntiagudo, se forman hermosos árboles plateados que continúan ramificándose. Siempre que utilice soluciones de electrolitos de baja concentración, se generará agua en el lado del ánodo o el material del ánodo en cuestión se oxidará. Sin embargo, si se aumenta la concentración de electrolito y se utiliza un material anódico inerte, como grafito o platino, se puede observar algo inesperado: también se forma un árbol fractal ramificado en el ánodo. ¿Cómo se puede explicar este fenómeno?
Para crear lo que parece un árbol plateado doble, primero debes configurar el experimento de acuerdo con la siguiente ilustración. Puede intercambiar los cables conductores utilizando pinzas de cocodrilo como polos negativo y positivo y cerrar el circuito. Agregue una solución de nitrato de plata de 1 mol/L a la placa de Petri. A continuación se realiza la electrólisis durante aproximadamente diez minutos a una tensión continua de diez voltios.
© Grupo de trabajo Marko Oetken, PH Freiburg (detalles)
Configuración de demostración | Para electrólisis de solución de nitrato de plata, c(AgNO3) = 1 mol/L, ánodo a la izquierda, cátodo a la derecha.
Ya al comienzo de la electrólisis se pueden observar en el cátodo (electrodo negativo) fractales de plata brillantes que crecen hacia el ánodo. Sin embargo, en el ánodo aparecen fractales de metal negro brillante que se extienden en una corriente hacia el cátodo.
© Grupo de trabajo Marko Oetken, PH Freiburg (detalles)
Árbol de cristal | 1) árbol de plata (cátodo); 2) Silver Tree con un aumento de aproximadamente 50x; 3) Hayy7No11-árbol (ánodo); 4) Hayy7No11-Árbol con un aumento aproximado de 50x.
Durante el experimento, los iones de plata (I) se reducen a plata elemental en el cátodo:
Cátodo: Ag+ (Aq) + mi– → Hayy(s)
Esto no es sorprendente dada la electrólisis de la solución de sal de plata que se realiza aquí. Pero lo inesperado es que se forme un sólido negro en el electrodo positivo. Se puede simplificar usando la fórmula de verano Ag7Ey11 Describir. Este compuesto complejo es un cristal mixto hecho de trióxido de plata (Ag3Ey4) con el porcentaje de nitrato de plata en total: Ag+yo(AG+En segundo lugarAG2+TerceroEy4)2No3. Como lo demuestran los análisis estructurales de rayos X, toda la Ag está presente en el complejo2+– Y cada Hajj3+Un ion rodeado por un cuadrado de cuatro átomos de oxígeno. Como AgO4-Las unidades están conectadas tridimensionalmente entre sí a través de esquinas y bordes comunes y pueden describirse como tetróxido de tri-plata con iones de plata divalentes y trivalentes: Ag+En segundo lugarAG2+TerceroEy4.
En las condiciones experimentales dadas, los iones de plata (I) de una solución de nitrato de plata se oxidan a iones de plata (II) y plata (III). También se crean iones de oxonio, que se pueden detectar mediante el indicador:
Ánodo: 7 Ag+ (Aq) + no3– (Ac) + 24 h2o(l) → [Ag+(Ag+IIAg2+IIIO4)2NO3–](s) + 16h3Ey+ (Aq) + 10AH–
La plata oxidada crece en el ánodo en estructuras ramificadas que se ramifican cada vez más. El requisito básico para ello es una buena conductividad eléctrica del compuesto de Ag.7No11. Por lo tanto, los iones de plata(I) se oxidan no sólo en el electrodo, sino también en las dendritas existentes. El mismo fenómeno es responsable del crecimiento de un árbol de plata en el cátodo: la plata primaria también conduce tan bien la electricidad que se forma otro fractal en el cátodo. La estructura ramificada en forma de árbol surge porque los iones de plata se mueven a través del electrolito en movimientos aleatorios mientras el producto (plata o Ag)7No11) se depositan periódicamente.
Después de la electrólisis se puede observar otro fenómeno interesante en el ánodo: en los fractales formados allí se forman burbujas de gas, que son particularmente fáciles de ver con un microscopio estereoscópico. Con el tiempo, los fractales se descomponen y existen sólo en partes.
© Grupo de trabajo Marko Oetken, PH Freiburg (detalles)
Formación de burbujas de gas. En el Hayy7No11-Plántula con un aumento de 50x después de la electrólisis.
La empresa combinada7No11Su estructura es térmicamente inestable y se descompone lentamente en iones de plata (I), iones de nitrato, monóxido de plata y oxígeno, incluso a temperatura ambiente. Este último se hace visible en forma de burbujas de gas:
Hayy(Hayy3Ey4)2No3 (s) → Hayy+ (Aq) + no3– (Aq) + 3 Haj+yoAG+TerceroEy2 (s) + s2 (gramo)
Las investigaciones térmicas han demostrado que esta descomposición se produce muy rápidamente y de forma muy exotérmica a una temperatura de 63°C, es decir, con desarrollo de calor. Esto se puede demostrar experimentalmente colocando la placa de Petri en una placa caliente después de la electrólisis y calentándola continuamente. A los pocos minutos se pueden ver muchas burbujas de oxígeno; Además, se puede observar directamente la descomposición de las dendritas.
© Grupo de trabajo Marko Oetken, PH Freiburg (detalles)
AG7No11-Las plántulas son térmicamente inestables. 1) el árbol a temperatura ambiente inmediatamente después de la electrólisis, 2) a temperatura ambiente tres minutos después de la electrólisis, 3) y 4) por analogía con calentamiento continuo a 63°C.
Cuando se forman fractales de óxido de plata, se crean iones de oxonio, lo que reduce el pH de la solución electrolítica. Esto se puede demostrar con un indicador adecuado durante la electrólisis, por un lado haciendo visible la reacción que se está produciendo y, por otro lado, resaltando los árboles con colores.
Para preparar la solución indicadora, agregue aproximadamente 5 ml de solución acuosa de rojo de metilo a la placa de Petri. Usando una pipeta desechable, agregue con cuidado la misma cantidad de solución de hidróxido de sodio (8 por ciento en peso de NaOH en agua) y ácido sulfúrico (10 por ciento en peso de H2).2Entonces4 en agua), de modo que el color amarillo anaranjado aparece poco antes del punto de transición a la zona ácida (color rojo). Luego se agrega el reactivo de detección a la solución de nitrato de plata y luego se realiza la electrólisis como se describe anteriormente.
Debido a la pequeña cantidad de solución indicadora en la placa de Petri y a la iluminación desde arriba a través del microscopio estereoscópico, la solución indicadora neutra aparece amarilla. Ya al comienzo de la electrólisis se puede observar cómo el color en la zona del ánodo cambia de amarillo a rojo. Este cambio de color «crece» con el árbol de óxido de plata. Debido a la iluminación y a la baja concentración del indicador, el color rojo aparece rosado bajo el microscopio. Sin embargo, no hay ningún cambio de color en el árbol plateado.
© Grupo de trabajo Marko Oetken, PH Freiburg (detalles)
Solución de nitrato de plata El rojo de metilo se añade después de la electrólisis y la formación de árboles metálicos. Diferentes colores muestran diferentes valores de pH. Izquierda: Hayy7No11-árbol; Derecha: Árbol de Plata.
Como se describió anteriormente, los iones de oxonio se forman como subproducto durante la oxidación de los iones de plata (I). Esto último se puede comprobar experimentalmente utilizando el indicador: una solución acuosa de rojo de metilo es amarilla con valores de pH superiores a 6,2 y rosa por debajo de pH 4,4. En la zona envolvente entre ellos, la solución indicadora está coloreada en naranja y amarillo.
Si agrega diferentes colorantes alimentarios a la solución de electrolitos, se pueden obtener imágenes sorprendentes: los fractales crecen sobre un fondo de color. Los colorantes utilizados son amarillo de quinoleína, azorpina, índigo carmín y verde lisamina B. Aquí también los colores aparecen diferentes debido a la pequeña cantidad en la placa de Petri y a la iluminación del microscopio estereoscópico, de modo que la solución teñida con azorrubina aparece rosada. De color rojo.
© Grupo de trabajo Marko Oetken, PH Freiburg (detalles)
En solución coloreada Las estructuras fractales se ven increíbles. 1) Silvertree, electrolito coloreado con amarillo de quinoleína; 2) Árbol de plata, electrolito coloreado con azorrubina; 3) Hayy7No11– Plántulas, índigo carmín teñidas con electrolitos; 4) Hayy7No11– Árbol de electrolitos coloreado con lisamina B verde.
Holtkemeyer, D., Oetken, M.: Consideraciones didácticas para implementar fenómenos de crecimiento controlado por difusión en lecciones de química. Shimcon 4/10, 2003
Standke, B., Janssen, M.: AG3Ey4, monóxido de plata (II, III). Química Aplicada 98, 1986
Standke, B., Janssen, M.: Representación y estructura cristalina de Ag.3Ey4. Revista de química del estado sólido 67, 1987
Wong, CH y otros: Redeterminación precisa de la estructura cristalina de Ag.7No11. Revista de Química Inorgánica y Nuclear 34, 1972
Permita que Javascript mantenga la funcionalidad completa de Spektrum.de.

«Alborotador. Amante de la cerveza. Total aficionado al alcohol. Sutilmente encantador adicto a los zombis. Ninja de twitter de toda la vida».